前言
2017年將是生技醫藥產業發展史上重要的一個年度,由於美國FDA核准上巿新藥數量創歷史新高,更通過3件基因治療新藥上市的核准,為生技醫藥產業發展的重大突破。另外,拜數位科技發展所賜,全球正處於邁向全面數位化,甚至是智慧化的時代,其生技醫療的運用更在法規逐步建置下,將加速數位醫療及精準醫療產業發展。創新科技的突破發展,以及數位化帶來行業破壞者的威脅進逼,使得生技醫藥產業面臨的挑戰不斷升高,到了必須重新思考商業模式的時候。
壹、從2018 BIO 洞察生技醫藥產業的新浪潮
每年在美國舉辦的BIO會展(BIO International Convention)是全球最大規模的生技醫藥產業年度盛會,世界各地的生技菁英滙聚於此洽談合作商機,並交流產業趨勢脈動,是觀測生技醫藥產業前瞻趨勢的重要聚點。2018年BIO適逢創始25周年,由大會觀測今年各大議題、超級論壇之內容,可從科技及政策/法規洞察生技醫藥產業的趨勢浪潮。
一、科技面
由於科技創新突破,能夠引領生技醫藥產業發展,從2018 BIO觀察,歸納主要熱議的科技議題包括生物技術的免疫療法(Immuno-therapy)、基因治療(Gene Therapy)、基因編輯(Gene Editing)、CAR-T細胞療法(CAR-T Cell Therapy)等細胞療法(Cell Therapy)和微生物組(Microbiome),以及數位科技的物聯網(IoT)(Internet of Things)、大數據(Big Data)、人工智慧(AI)等。
二、政策/法規面
因為生技醫藥產業具高度法規規範的特質,因此新制定之法規關乎生技醫藥產品能否順利取得上巿資格,以及廠商是否能夠取得認證資格等,將影響生技醫藥產業發展的速度。重點之政策/法規包括:
(一)精準醫療倡議(Precision Medicine Initiatives, PMI)
美國前總統歐巴馬在2015年國情咨文演說中提出的「精準醫療倡議」(Precision Medicine Initiatives, PMI),正式開啟了精準醫療革命,各國紛紛積極投入發展精準醫療。其概念主要是將疾病更精緻、科學化地分類,透過資料庫比對及分析個體的體學及外源性數據,以進行精準化之疾病診斷、分類,並選擇最適合的治療方案及藥品,達到治療最佳化,長期目標則是期待做到預測及預防疾病。
(二)21世紀治癒法案(21st Century Cures Act)
美國國會於2016年12月所通過的《21世紀治癒法案》(21st Century Cures Act),主要為鼓勵高價值、具突破性的創新藥品上市,以及支持精準醫療研究,探究疾病與個體基因間的關聯,並簡化美國FDA之審查程序與優化法規監管品質,進而影響2017年後有關數位醫療及再生醫療的法規訂定及後續產業發展。
(三)再生醫療先進療法(RMAT)
美國FDA自2017年3月開始施行《再生醫療先進療法》(Regenerative Medicine Advanced Therapy, RMAT)認證,提供符合再生醫療先進療法認證的產品加速審查機制;11月再頒布細胞及再生醫療產品的政策性框架以進一步對細胞治療產業進行監督管理,同時規範廠商之細胞及再生醫療產品設計與開發。
(四)數位醫療相關法規的建置
為促進數位醫療安全並有效之創新活動,美國FDA於2017年7月提出「數位醫療創新行動方案」(Digital Health Innovation Action Plan),鼓勵藥品與數位健康科技之創新,8月更公布《使用真實世界證據以支持醫療器材查驗登記指引》(Use of Real-World Evidence to Support Regulatory Decision-Making for Medical Devices),正式將「真實世界證據(Real-World Evidence, RWE)」納入作為美國FDA在審查時的參考資料之一;11月再發表聲明指出,將鬆綁目前對於消費型基因檢測(Direct-to-Consumer, DTC)的審查標準,以協助產業加速提供安全、有效且創新的基因檢測產品給消費大眾;然而歐盟EMA制定新的《數據隱私法》(General Data Protection Regulation, GDPR 2018),希望在開放數位醫療產業發展的同時,能先確保數據取得及運用之安全性,此法規的制定,將可能對大數據的運用產生不利的影響。
貳、新浪潮影響生技醫藥未來產業樣貌
一、新產品上巿的重大突破,影響生技醫藥產業未來樣貌
美國FDA在2017年核准了多項具產業重大突破意義的創新產品,將扮演生技醫藥產業的未來發展關鍵。
(一)基因治療時代來臨
美國FDA在2017年相繼核准了3件基因治療藥物,分別是8月30日首度核准Novartis的CAR-T細胞療法(Kymriah)上巿,是人類首度將取出人體的免疫細胞進行基因改造並增殖後,再送回人體進行癌症免疫療法的基因治療產品被美國FDA核准上巿;10月18日核准Gilead Sciences的CAR-T細胞治療藥物Yescarta上巿;12月19日則核准首例遺傳性視網膜疾病的基因治療藥物Luxturna,為直接利用病毒載體將修復基因注射至遺傳性視網膜疾病患者的眼睛,讓遺傳性失明的幼童重見光明。基因治療藥物成功上巿,將產業發展推向另一個新時代,相關研究大量崛起,基因治療臨床試驗數從2015年的100件爆增至2017年的250件以上。
(二)精準醫療在2017年取得重大突破
美國FDA在2017年5月23日核准全球首例以特有生物標記作為病患篩選的依據,而非以適應症來決定治療方式,針對攜帶有MSI-H(Microsatellite Instability-High,微衛星不穩定高)或dMMR(Mismatch Repair deficient,錯誤配對修復缺乏)生物標記之各種實體腫瘤患者可使用Keytruda治療。
FDA在4月6日核准23andMe公司銷售基因檢測Personal Genome Service Genetic Health Risk產品,為美國首例獲准之消費型基因檢測(Direct-to-Consumer, DTC)產品。可不經醫生處方而訂購個人基因組的客製化遺傳分析報告。此產品是以美國FDA Pre-Cert新醫療器材上市前審查途徑(De Novo Premarket Review Pathway)進入巿場,為消費者基因檢測發展史上的重大里程碑。
另外,11月30日美國FDA核准Foundation Medicine的NGS基因檢測試劑FoundationOne CDx(F1CDx)上市,為首例綜合基因組分析測試(Comprehensive Genomic Profiling)之NGS體外診斷試劑,亦是第二例獲FDA核准的NGS伴隨式診斷產品,可檢測實體腫瘤的324個基因遺傳變異和兩個基因組標記(MSI, TMB),F1CDx同時取得美國聯邦醫療保險和補助服務中心(Centers for Medicare & Medicaid Services, CMS)發布之NGS檢測國家給付標準(National Coverage Determination, NCD),建議將F1CDx納入Medicare的醫保給付覆蓋目錄,不但為癌症精準醫療檢測的重要里程碑,更加速NGS檢測產品之臨床應用發展。
(三)數位醫療的創新產品
美國FDA於2017年11月13日核准首例數位藥丸,為大塚製藥(Otsuka)與Proteus數位健康公司所開發製造之Abilify MyCite(aripiprazole含感測器),為思覺失調症藥品Abilify結合感測器製成,當與胃酸接觸時可產生電訊號傳到患者身上的貼片,再將服用時間和劑量等數據傳送至手機供參考,可追蹤病患用藥情況。
此外,於9月14日FDA再核准首款需處方才能使用之手機數位App,稱為數位處方療法產品,為Pear Therapeutics所開發之APP-reSET,用於藥物成癮的輔助治療。此款數位軟體是使用認知行為療法(Cognitive Behavioral Therapy, CBT)協助藥物成癮的患者避免藥物濫用,提高其持續進行治療的機率。
二、生技醫藥產業之未來樣貌
根據上述的新浪潮觀測,預測生技醫藥產業的未來樣貌,由供給面至需求面整理觀察如下:
(一)由藥物轉變為療法
過去的藥物治療,在創新科技突破下,由傳統小分子藥品,典範轉移至以抗體藥物為主的生物藥品時代,現因創新的基因療法、細胞療法取得重要突破性進展,在臨床上提高治癒的可能性,可能由過去的持續性治療,轉變為一次性治療;此外,過去是由藥物提供治療,產業研發、製造藥物以供應醫療所需,將轉變為更為複雜化的生物治療方式,是一種療法,再加上數位化發展,醫療的提供將趨於複雜化,生技醫藥產業價值鏈與供應鏈將因此複雜度增高。
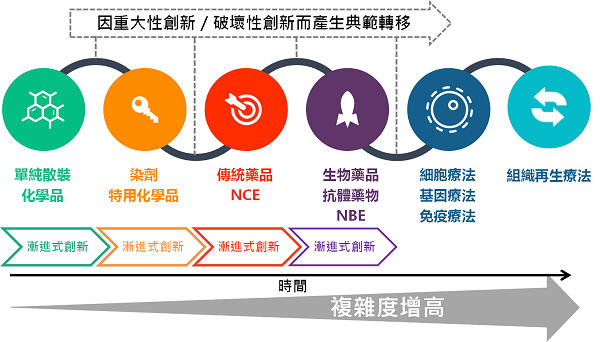 創新技術突破產生生技醫藥產業之典範轉移/資料來源:DCB產業資訊組整理
創新技術突破產生生技醫藥產業之典範轉移/資料來源:DCB產業資訊組整理
(二)全面數位化的生技醫藥產業
未來的生技醫藥產業在政府為控制醫療支出,科技發達使得病人賦權增高及精準醫療的需求下,未來將講究醫療成效,並在數位科技的推波助瀾下,趨於多元複雜的產業價值鏈與供應鏈管理將朝向數位化創新,成為全面數位化的醫藥4.0時代,以數據為導向的平臺。顧客不再只限於醫療/護理提供者或支付方,將是多樣化的病患/消費者、政策制定者、支付方或醫療/護理提供者。然而全面數位化將使得數據泛濫,因此數據品質要求的提高是數位醫療發展的關鍵成功要素。
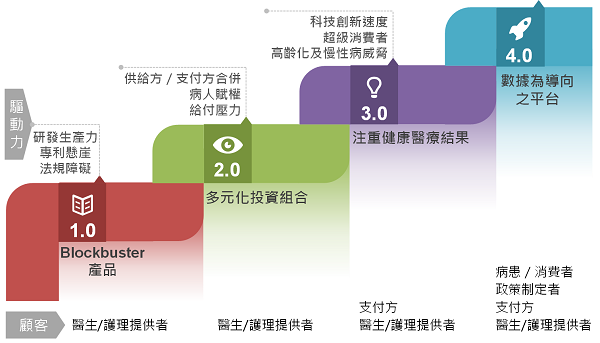 新浪潮迫使產業轉型為醫藥4.0/資料來源:DCB產業資訊組整理
新浪潮迫使產業轉型為醫藥4.0/資料來源:DCB產業資訊組整理
(三)醫療生態系轉變
精準醫療及數位醫療的發展,將使得醫療生態系因而轉變,生技醫藥產業原本提供給醫師診斷到治療的傳統模式,將因精準醫療的療效提高的要求,而受到挑戰,並且在全面數位化導入下,醫療生態系進入變動及重塑時期。
(四)獲利模式翻轉
過去暢銷藥物的藥廠獲利模式,在醫藥4.0的生技醫藥產業時代將難再現,對於治療結果的注重,使得醫療改革將以價值提供為關鍵評估及支付重點,「論治療效果計酬」的給付模式興起,企業的商業模式將可能因此翻轉。
(五)病人參與度增高
由於數位科技及資訊發達,使病人參與度增高,民眾對就醫權益的要求高漲,以及真實世界數據的全面導入,所以,在過去的醫療需求及供給面關係是由藥廠供給、醫療照護者決策的單向時代,將轉而以「實證健康照護」及「共同決定」的未來模式發展。
叁、生醫企業生命週期將面臨變革
一、企業面臨效率低下困境及行業破壞者的威脅
近二十年來,藥廠在新藥研發效率降低、現有賴以成功的暢銷藥物商業模式已面臨投資報酬率每況愈下的困境,進入一個銷售增長萎縮、營收下滑,因而調降研發支出的惡性循環,企業必須打破現有商業模式,因應新時代的轉變,轉型至創新的獲利模式,再創成長動能。
此外,數位醫療時代來臨、醫療生態系重塑的過程中,如Google、IBM、Facebook等科技大廠動作頻頻地投入生技醫療生態系,甚至切入到生技醫藥產業供應鏈,藥廠將因鏈條被截入而威脅到其盈利能力。
二、生技醫藥產業和科技業的競合
生技企業與科技大廠在未來的生技醫藥產業發展是敵或是友?必須從競爭策略角度去瞭解。藥廠向來是專注於提供病患治療產品,透過服務醫生治療病患,因具備對疾病的專業理解,受到支付者的信賴,並且已有豐富的法規監管經驗,並有醫藥專業經銷能力及通路關係。藥廠在面臨投資報酬率下滑的瓶頸下,已多透過轉向提供更多附加價值,並趨向以病患為中心的服務模式,以提高營收,將來更可能擴及服務至消費大眾,以增加收入來源。
科技大廠一向以研發、生產一般消費產品,其顧客為一般消費者,是以人為中心的服務導向,具靈活、彈性、快速之優勢,由於專注於服務,因此與消費者連結緊密,擁有豐富的整合、連結經驗,現在挾著掌握消費者端的大量數據,發展數位醫療產品與服務,未來將由大數據切入真實世界數據對疾病專業理解與研究,開發出創新的醫療解決方案或產品。
因此,在競合關係上,生技企業是由病患端的客戶,切入健康管理、加值服務及預防醫學以擴大至未病之顧客對象;另一方的科技廠商則是由一般消費者切入消費者基因檢測、健康管理、慢性病產品及服務等,進入醫療領域。若能夠透過競合策略找到優勢互補的合作機會,便能產生緃效,發揮槓桿力量。
結論與建議
面對生技醫藥產業的變革浪潮來襲,在基因治療、精準醫療和數位醫療的未來趨勢,產品不再僅止是藥品,而是結合多元科技創新的產品、平台、服務的全方位治療或健康維持方案,未來須致力於「病人愈健康,營運就愈好」的價值提供。
當藥價成為醫療支出的壓力來源,過去的獲利模式已不再能滿足企業成長需求,布局新獲利來源以維持/提高營收已是必然,傳統研發至製造的獲利模式將轉變為產品結合服務供應的獲利模式,滿足服務之需求為新興布局契機。未來生技醫藥產業的商業模式依企業定位及發展策略,大約可分為四類:(1)突破性創新者;(2)疾病管理者;(3)高效生產者;(4)健康生活管理者。
 生技醫藥產業的未來商業模式/資料來源:DCB產業資訊組整理
生技醫藥產業的未來商業模式/資料來源:DCB產業資訊組整理
建議臺灣生技醫藥產業在醫療生態系藉新遊戲規則重建時期,須找到自身的差異化競爭力,透過洞察醫療及產業新運作結構,找到獲利的關鍵目標客戶,並滿足客戶需求,提供附加價值,從國際企業新商業模式的價值鏈或供應鏈之策略聯盟切入點,卡位國際鏈結的利益關係者的網絡,才能為自己的產業找到新立足點。
參考資料
- FDA approves first cancer treatment for any solid tumor with a specific genetic feature,https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm560167.htm
- FDA approval brings first gene therapy to the United States,https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm574058.htm
- FDA approves CAR-T cell therapy to treat adults with certain types of large B-cell lymphoma,https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm581216.htm
- FDA approves novel gene therapy to treat patients with a rare form of inherited vision loss,https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm589467.htm
- FDA allows marketing of first direct-to-consumer tests that provide genetic risk information for certain conditions,https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm551185.htm
- FDA announces approval, CMS proposes coverage of first breakthrough-designated test to detect extensive number of cancer biomarkers,https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm587273.htm
- FDA approves pill with sensor that digitally tracks if patients have ingested their medication,https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm584933.htm
- FDA permits marketing of mobile medical application for substance use disorder, https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm576087.htm
- Morrison C (2018) C Morrison Fresh from the biotech pipeline—2017. Nat Biotechnol, 35(2):108-112
- Statement from FDA Commissioner Scott Gottlieb, M.D., on implementation of agency’s streamlined development and review pathway for consumer tests that evaluate genetic health risks,https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm583885.htm
- The Personalized Medicine Coalition (PMC), (2018) Personalized Medicine at FDA 2017 Progress Report
- 財團法人生物技術開發中心(2018)2018醫藥產業年鑑
- 賴瓊雅, 鄭宇婷, 劉曉君(2016).伴同式診斷於藥物開發之發展模式及商機探討